ການຟື້ນຟູຂອງຫມໍ້ໄຟ sodium-ion ອຸນຫະພູມຫ້ອງ
ເນື່ອງຈາກສະຫງວນໂຊດຽມ (Na) ທີ່ອຸດົມສົມບູນຢູ່ໃນເປືອກໂລກແລະຄຸນສົມບັດທາງເຄມີທາງກາຍະພາບທີ່ຄ້າຍຄືກັນຂອງໂຊດຽມແລະ lithium, ການເກັບຮັກສາພະລັງງານໄຟຟ້າທີ່ໃຊ້ໂຊດຽມຖືສັນຍາທີ່ສໍາຄັນສໍາລັບການເກັບຮັກສາພະລັງງານຂະຫນາດໃຫຍ່ແລະການພັດທະນາຕາຂ່າຍໄຟຟ້າ. ຕົວຢ່າງເຊັ່ນ, ເຊັລຄົ້ນຄວ້າກິດຈະກໍາຂອງແບັດເຕີລີການປ່ອຍອາຍພິດອຸນຫະພູມສູງທີ່ອີງໃສ່ລະບົບ Na/NiCl2 ແລະເຊລ Na-S ທີ່ມີອຸນຫະພູມສູງ, ເຊິ່ງເປັນກໍລະນີທາງການຄ້າທີ່ປະສົບຜົນສຳເລັດຂອງການນຳໃຊ້ສະຖານີ ແລະ ມືຖື, ໄດ້ສະແດງໃຫ້ເຫັນເຖິງທ່າແຮງຂອງແບັດເຕີຣີທີ່ສາມາດສາກດ້ວຍໂຊດຽມແລ້ວ. ຢ່າງໃດກໍ່ຕາມ, ອຸນຫະພູມການເຮັດວຽກສູງຂອງພວກມັນປະມານ 300 °C ເຮັດໃຫ້ເກີດບັນຫາຄວາມປອດໄພ ແລະຫຼຸດລົງປະສິດທິພາບການໄປມາຂອງແບດເຕີຣີໂຊດຽມ-ໄອອອນ (SIBs). ດັ່ງນັ້ນ, SIBs ອຸນຫະພູມຫ້ອງ (RT) ຖືກຖືວ່າເປັນເຕັກໂນໂລຢີທາງເລືອກທີ່ໂດດເດັ່ນທີ່ສຸດສໍາລັບ LIBs.
ໃນໄລຍະປະຫວັດສາດຂອງຫມໍ້ໄຟໃນ 200 ປີທີ່ຜ່ານມາ, ການຄົ້ນຄວ້າກ່ຽວກັບ SIBs ໄດ້ຖືກປະຕິບັດຢ່າງຈິງຈັງກັບການພັດທະນາ LIB. ກິດຈະກໍາ electrochemical ຂອງ TiS2 ສໍາລັບ lithium ແລະຄວາມເປັນໄປໄດ້ຂອງມັນສໍາລັບການເກັບຮັກສາພະລັງງານໄດ້ຖືກວາງໄວ້ຄັ້ງທໍາອິດໃນຊຸມປີ 1970. ຫຼັງຈາກການຄົ້ນພົບນີ້, ຄວາມສາມາດຂອງ Na ions ທີ່ຈະໃສ່ເຂົ້າໄປໃນ TiS + 2 ໄດ້ຖືກຮັບຮູ້ໃນຕົ້ນຊຸມປີ 1980. ດ້ວຍການຄົ້ນພົບຂອງ graphite ເປັນວັດສະດຸ anode ທີ່ມີລາຄາຖືກແລະປານກາງສໍາລັບ LIBs ແລະຄວາມລົ້ມເຫຼວທີ່ຈະ intercalate sodium ions, ການພັດທະນາ LIB ຢ່າງໄວວາໄດ້ເກີດຂຶ້ນໃນຊຸມປີ 1990, ແທນການຂະຫຍາຍຕົວໃນເຄມີສາດ sodium. ຫຼັງຈາກນັ້ນ, ໃນປີ 2000, ຄວາມພ້ອມສໍາລັບການເກັບຮັກສາໂຊດຽມໃນຄາບອນແຂງ (HC), ເຊິ່ງຈະເຮັດໃຫ້ຄວາມສາມາດໃນການພະລັງງານທີ່ຄ້າຍຄືກັບ Li ໃນ graphite, ມີຄວາມສົນໃຈໃນການຄົ້ນຄວ້າຂອງ SIBs ຟື້ນຟູ.
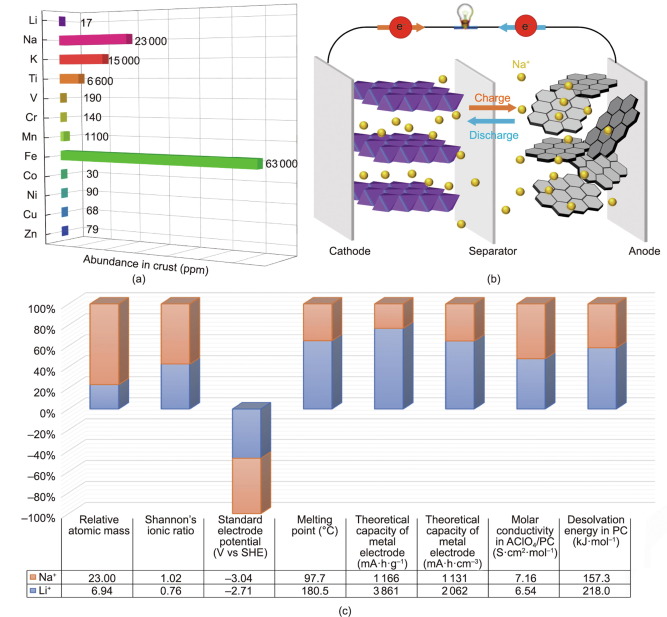
ການປຽບທຽບຫມໍ້ໄຟ Sodium-ion ແລະຫມໍ້ໄຟ Lithium-ion
ການຟື້ນຟູຂອງ SIBs - ບວກໃສ່ກັບຄວາມກົດດັນທີ່ເພີ່ມຂຶ້ນຢ່າງຕໍ່ເນື່ອງຈາກການຂາດການມີສະຫງວນໄວ້ຂອງ lithium ແລະການເພີ່ມຂື້ນຂອງຄ່າໃຊ້ຈ່າຍທີ່ສອດຄ້ອງກັນ - ສະຫນອງຍຸດທະສາດເສີມໃຫ້ກັບ LIBs. SIBs ໄດ້ຮັບຄວາມສົນໃຈໃນການຄົ້ນຄວ້າເພີ່ມຂຶ້ນ, ສົມທົບກັບຜົນສໍາເລັດພື້ນຖານຂອງວິທະຍາສາດວັດສະດຸ, ໃນການຂັບເຄື່ອນເພື່ອຕອບສະຫນອງການເພີ່ມຂຶ້ນຂອງເຕັກໂນໂລຊີພະລັງງານທົດແທນ. ອົງປະກອບຂອງເຊນ ແລະກົນໄກປະຕິກິລິຍາທາງເຄມີຂອງ SIB ໂດຍພື້ນຖານແລ້ວແມ່ນຄ້າຍຄືກັນກັບ LIBs, ຍົກເວັ້ນຕົວເກັບຄ່າ, ເຊິ່ງແມ່ນ Na ໃນໜຶ່ງ ແລະ Li ໃນອີກອັນໜຶ່ງ. ເຫດຜົນຕົ້ນຕໍສໍາລັບການຂະຫຍາຍອອກຢ່າງໄວວາໃນວັດສະດຸເຄມີຂອງ SIB ແມ່ນຫມາຍເຖິງຄວາມຂະຫນານໃນຄຸນສົມບັດທາງກາຍະພາບລະຫວ່າງສອງໂລຫະທີ່ເປັນດ່າງ.
ຫນ້າທໍາອິດ, ຫຼັກການການດໍາເນີນງານແລະການກໍ່ສ້າງຈຸລັງຂອງ SIBs ແມ່ນຄ້າຍຄືກັນກັບ LIBs ການຄ້າ, ເຖິງແມ່ນວ່າ Na ໃຫ້ບໍລິການເປັນຜູ້ໃຫ້ບໍລິການ. ສີ່ອົງປະກອບຕົ້ນຕໍມີຢູ່ໃນ SIB ທົ່ວໄປ: ວັດສະດຸ cathode (ປົກກະຕິແລ້ວເປັນສານປະສົມ Na-containing); ວັດສະດຸ anode (ບໍ່ຈໍາເປັນຕ້ອງປະກອບດ້ວຍ Na); electrolyte (ໃນສະພາບຂອງແຫຼວຫຼືແຂງ); ແລະຕົວແຍກ. ໃນລະຫວ່າງຂະບວນການສາກໄຟ, ໂຊດຽມ ions ຖືກສະກັດອອກຈາກ cathodes, ເຊິ່ງປົກກະຕິແລ້ວແມ່ນຊັ້ນໂລຫະ oxides ແລະທາດປະສົມ polyanionic, ແລະຫຼັງຈາກນັ້ນຖືກໃສ່ເຂົ້າໄປໃນ anodes, ໃນຂະນະທີ່ກະແສໄຟຟ້າເຄື່ອນຍ້າຍຜ່ານວົງຈອນພາຍນອກໃນທິດທາງກົງກັນຂ້າມ. ເມື່ອປ່ອຍອອກ, Na ອອກຈາກ anodes ແລະກັບຄືນສູ່ cathodes ໃນຂະບວນການທີ່ເອີ້ນວ່າ "ຫຼັກການຂອງເກົ້າອີ້." ຄວາມຄ້າຍຄືກັນເຫຼົ່ານີ້ໄດ້ເຮັດໃຫ້ຄວາມເຂົ້າໃຈເບື້ອງຕົ້ນແລະການຂະຫຍາຍຕົວຢ່າງໄວວາໃນເຕັກໂນໂລຢີ SIB.
ຍິ່ງໄປກວ່ານັ້ນ, ລັດສະໝີ ionic ທີ່ໃຫຍ່ກວ່າຂອງ Na ເອົາຂໍ້ໄດ້ປຽບຂອງຕົນເອງ: ຄວາມຍືດຫຍຸ່ນເພີ່ມຂຶ້ນຂອງ electrochemical positivity ແລະການຫຼຸດລົງຂອງພະລັງງານ de-solvation ໃນສານລະລາຍຂົ້ວໂລກ. ຊ່ອງຫວ່າງຫຼາຍກວ່າເກົ່າໃນລັດສະໝີ ionic ລະຫວ່າງ Li ແລະ ions ໂລຫະທີ່ຫັນປ່ຽນມັກຈະນໍາໄປສູ່ຄວາມລົ້ມເຫຼວຂອງຄວາມຍືດຫຍຸ່ນຂອງການອອກແບບວັດສະດຸ. ໃນທາງກົງກັນຂ້າມ, ລະບົບທີ່ອີງໃສ່ໂຊດຽມເຮັດໃຫ້ໂຄງສ້າງແຂງທີ່ມີຄວາມຍືດຫຍຸ່ນຫຼາຍກ່ວາລະບົບທີ່ອີງໃສ່ lithium, ແລະມີ conductivity ionic ຢ່າງຫຼວງຫຼາຍ. ຕົວຢ່າງປົກກະຕິແມ່ນ β-Al2O3, ເຊິ່ງ Na intercalation ມີຂະຫນາດທີ່ສົມບູນແບບແລະປະສິດທິພາບສູງ. ທາດຜຸພັງຂອງໂລຫະທີ່ປ່ຽນເປັນຊັ້ນຫຼາຍດ້ວຍວິທີການຈັດວາງ M+x+ ທີ່ແຕກຕ່າງກັນສາມາດຮັບຮູ້ໄດ້ງ່າຍໃນລະບົບທີ່ໃຊ້ໂຊດຽມ. ເຊັ່ນດຽວກັນ, ຄວາມຫລາກຫລາຍຂອງໂຄງສ້າງໄປເຊຍກັນທີ່ເປັນທີ່ຮູ້ຈັກສໍາລັບຄອບຄົວຂອງ sodium ionic conductor (NaSICON) ແມ່ນສັບສົນຫຼາຍກ່ວາຂອງ analogs lithium. ສິ່ງທີ່ ສຳ ຄັນກວ່ານັ້ນ, ການ ນຳ ໃຊ້ ionic ທີ່ສູງກວ່າສາມາດຖືກອະນຸຍາດໃນທາດປະສົມ NaSICON, ເຊິ່ງເກີນກວ່າການ ນຳ ໃຊ້ ionic ໃນທາດປະສົມ lithium ionic conductor (LiSICON).
ສຸດທ້າຍແຕ່ບໍ່ໄດ້ຢ່າງຫນ້ອຍ, ການສືບສວນລະບົບທີ່ມີສານລະລາຍຂົ້ວໂລກ aprotic ທີ່ແຕກຕ່າງກັນໄດ້ສະແດງໃຫ້ເຫັນວ່າລັດສະຫມີ ionic ທີ່ໃຫຍ່ກວ່າຂອງ Na ເຮັດໃຫ້ພະລັງງານ desolvation ອ່ອນແອລົງ. Li ຂະຫນາດນ້ອຍກວ່າມີຄວາມຫນາແຫນ້ນຂອງຄ່າໃຊ້ຈ່າຍດ້ານຫນ້າຂອງແກນສູງກວ່າ Na ໃນເວລາທີ່ທັງສອງມີ valence ດຽວກັນ. Li ແມ່ນເພາະສະນັ້ນຈຶ່ງເຮັດໃຫ້ຄວາມຫມັ້ນຄົງຂອງ thermodynamically ໂດຍການແບ່ງປັນເອເລັກໂຕຣນິກເພີ່ມເຕີມກັບໂມເລກຸນລະລາຍຂົ້ວໂລກ. ນັ້ນແມ່ນ, Li ສາມາດຖືກຈັດປະເພດເປັນອາຊິດ Lewis. ດັ່ງນັ້ນ, ພະລັງງານ desolvation ຂ້ອນຂ້າງສູງແມ່ນຈໍາເປັນສໍາລັບ Li ຂົ້ວສູງ, ນໍາໄປສູ່ການຕໍ່ຕ້ານການໂອນຂະຫນາດໃຫຍ່ຂ້ອນຂ້າງຖືກ induced ໂດຍການຂົນສົ່ງຂອງ Li ຈາກລັດຂອງແຫຼວ (electrolyte) ກັບລັດແຂງ ( electrode). ເນື່ອງຈາກພະລັງງານ desolvation ແມ່ນກ່ຽວຂ້ອງຢ່າງໃກ້ຊິດກັບ kinetics ການໂອນທີ່ເກີດຂື້ນໃນການໂຕ້ຕອບຂອງແຫຼວ / ແຂງ, ພະລັງງານ desolvation ທີ່ຂ້ອນຂ້າງຕໍ່າແມ່ນເປັນປະໂຫຍດທີ່ສໍາຄັນສໍາລັບການອອກແບບ SIBs ທີ່ມີພະລັງງານສູງ.